人才强校 | 王军军教授课题组在功能配料缓解肠道炎症及其菌群介导黏膜屏障与固有层巨噬细胞重建方面取得重要进展
本网讯 近日,我校动物科技学院王军军教授在国际知名学术期刊《Gut Microbes》在线发表了题为 “Cohousing-mediated microbiota transfer from milk bioactive components-dosed mice ameliorate colitis by remodeling colonic mucus barrier and lamina propria macrophages” 的最新研究成果( https://doi.org/10.1080/19490976.2021.1903826 )。
宫内生长受限(Intrauterine Growth Restriction, IUGR)导致仔猪生命早期死亡率高、后期生长性能低,对其肠道发育缺陷与养分利用特征认知不足是制约IUGR猪营养调控有效性的关键。为此,王军军教授课题组长期从事IUGR猪肠道结构功能缺陷、炎症发生发展、微生物差异定植及其营养干预研究。基于前期研究发现乳脂球膜、低聚半乳糖和低聚果糖组合而成的功能配料(CMFG)具有强大益生作用,本研究进一步系统探索了CMFG对机体肠道屏障功能、肠道菌群以及炎症反应的改善作用,并通过共养介导肠道微生物转移和肠道微环境重构,揭示了微生物移植缓解肠道炎症的效果与机制。
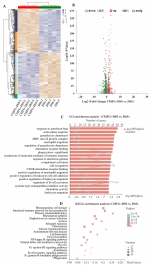
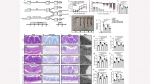
首先,作者基于葡聚糖硫酸钠(DSS)诱导的小鼠结肠炎模型,发现预添加CMFG显著改善结肠组织形态和肠道紧密连接,促进结肠杯状细胞增殖及其黏蛋白MUC2分泌(图1),改善肠道屏障功能相关基因表达(图2),抑制促炎基因表达上调和TLR4信号通路过度激活,并抑制肠道上皮细胞凋亡和结肠固有层促炎巨噬细胞极化。同时,CMFG可促进短链脂肪酸产生菌(如艾克曼菌、乳酸菌和罗斯菌)的增殖,并通过增加乙酸和丁酸产生、改善肠道黏膜屏障、抑制肠道上皮细胞凋亡和氧化损伤等方式发挥益生作用,进而缓解小鼠结肠炎(图1)。因此,肠道微生物在CMFG缓解小鼠结肠炎方面或扮演着不可或缺的角色。
为进一步验证功能配料CMFG的益生作用,作者利用小鼠共养模型,发现CMFG干预后的肠道菌群可被成功移植至受体小鼠,在一定程度上恢复了受体小鼠结肠黏膜屏障完整性(图3),并通过传递艾克曼菌等短链脂肪酸产生菌(图4),使受体小鼠再现缓解肠道炎症表型。
本研究以肠道微生物和上皮细胞互作为切入点,首次发现添加低聚糖与乳脂球膜等功能配料组合可通过增加短链脂肪酸产生菌的定植、促进杯状细胞增殖及其黏蛋白MUC2分泌而改善肠道微生态和黏膜屏障,减少结肠固有层促炎巨噬细胞而改善肠道免疫微环境,进而缓解肠道炎症;且通过混养建立菌群水平传递后,受体鼠成功再现了上述表型,验证了肠道微生物在功能配料改善肠道稳态和缓解炎症方面的介导作用,为仔猪营养优化提供了新思路。
我校动物科技学院王军军教授为论文通讯作者,动物科技学院2018届硕士毕业生刘聪(现为荷兰莱顿大学医学中心博士研究生)和2019届博士毕业生黄世猛(现为江苏省农业科学院和圣路易斯华盛顿大学医学院联合培养博士后)为论文共同第一作者。我校动物医学院张冰老师在动物实验开展方面提供了大力支持,美国阿肯色大学赵江潮老师对论文给予了指导和帮助。该工作获得了国家自然科学基金、北京市自然科学基金和111创新引智基地等项目的资助。