人才强校 | 生物学院吴森教授、赵要风教授团队在哺乳动物克隆胚胎早期流产机制研究中取得重要进展
本网讯 近日,我校生物学院吴森教授和赵要风教授团队在哺乳大动物早期流产机制研究中取得重要进展,相关研究在线发表于国际知名期刊《PNAS》,文章题目为“Silencing of Retrotransposon-derived Imprinted Gene RTL1 is the Main Cause for Post-implantational Failures in Mammalian Cloning”,该研究揭示了内源逆转录病毒来源的父本印记基因RTL1是影响哺乳动物早期流产的关键基因,通过对其表达的控制,可以显著地提高哺乳大动物克隆胚胎受体的怀孕率。
自从第一头克隆哺乳动物克隆羊“多利”诞生以来,核移植克隆技术取得了长足的发展,但是哺乳动物克隆的效率依然处于很低水平,比如克隆小鼠的效率为1-2%,克隆绵羊的效率为0.3%,克隆马的效率为0.8%,克隆牛的效率为1.7%,克隆猴的效率为1.5%,操作流程和培养体系相对成熟的克隆猪的效率也只处在0.3%左右的水平,更有甚者,iPS细胞克隆猪的效率几乎接近0%。换言之,也就是大约99%的克隆胚胎并没有发育至成熟个体,在妊娠期的各个阶段出现了大规模的流产现象。表观遗传重编程是核移植重编程过程中重要的一环,表观遗传重编程异常与核移植效率低下密切相关,但是其具体机制并不清晰。
该研究将猪iPS细胞克隆胚胎作为研究大型哺乳动物克隆胚胎流产的一种特殊模型,并运用西方猪种杜洛克和中国地方猪种荣昌猪进行杂交,取其子一代的胎儿成纤维细胞、iPS细胞,以及这两种细胞来源的克隆胎儿和胎盘,进行了全基因组的甲基化和链特异性转录组分析,通过对影响猪植入后胚胎发育相关印记基因的鉴定和分析,该团队锁定了基因组DLK1-DIO3是影响流产的关键区域,并且该区域中一个编码蛋白印记基因RTL1处于异常的高甲基化状态,通过对RTL1进行剂量补偿表达之后,该团队高效率地获得了iPS细胞克隆猪。并且通过更广泛的大规模数据分析发现印记基因RTL1的异常表达与猪牛的体细胞克隆胚胎附植后发育异常,大小鼠和人的多能干细胞的多能性,以及人早期胎儿流产密切相关。
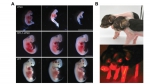
(A) 妊娠期第25天,iPS细胞克隆猪胎儿、RTL1补偿表达的iPS细胞克隆猪胎儿、自然受精猪胎儿的形态照片;(B) 一周龄大iPS细胞克隆猪仔的形态照片。
我校吴森教授、赵要风教授、杜旭光博士,以及我校荣誉教授、2007年诺贝尔生理或医学奖获得者Mario Capecchi是论文共同通讯作者,博士后工作人员余大为、王靖、邹惠影、冯涛为论文的共同第一作者,该研究得到了国家转基因重大专项、国家高技术研究发展计划,以及我校111引智计划、农业生物技术国家重点实验室校外科学家项目、北京市食品营养与人类健康高精尖创新中心开放基金项目的支持。